传染性法氏囊病毒解决方案
一、传染性法氏囊病毒流行趋势

1.1
超强毒株的出现与持续流行

vvIBDV:自20世纪80年代末被发现以来,超强毒力型传染性法氏囊病毒 已成为全球范围内的主导流行毒株。这类毒株引起的死亡率可高达60%-70%,法氏囊出血和萎缩更为严重,造成的免疫抑制也更强。
vvIBDV的演化:最初的vvIBDV主要集中在中国、日本、东南亚、欧洲等地,但现在已遍布全球主要养鸡地区,并且其本身也在不断发生遗传演化,产生新的亚分支。
1.2
新型变异株的涌现

这是当前最令人担忧的趋势之一。这类毒株的抗原性发生了改变,能够突破传统疫苗提供的保护。
抗原变异株:例如美国的VarE、VarA,以及中国的G2型等。这些毒株:
不引起典型的高死亡率:临床症状和病变不明显,容易被忽视。
但导致严重的、长期的免疫抑制:鸡群看起来“健康”,但生长迟缓,对疫苗应答差,易发继发感染,造成巨大的经济损失。
“隐形”流行:由于缺乏典型症状,往往在通过实验室监测时才被发现。
1.3
宿主范围与临床表现的扩大

发病日龄拓宽:传统认为3-6周龄是易感期,但现在早至10日龄以内,晚至产蛋期的鸡群都有发病的报道。这给免疫程序的制定带来了巨大困难。
非典型病例增多:很多感染表现为亚临床症状,仅见生产性能下降和免疫抑制,而看不到法氏囊的典型出血肿胀。
1.4
疫苗与野毒之间的“军备竞赛”

免疫压力下的病毒演化:一方面,IBDV是RNA病毒,容易在动物体内复制过程中不断发生变异或者与田间野毒重组产生重组毒;另一方面,为了控制vvIBDV,养殖场普遍使用中等偏强毒力的活疫苗。这种广泛的免疫压力筛选出了能够逃逸疫苗免疫保护的变异毒株。
疫苗选择不当的风险:在流行变异株的地区,如果仅使用经典毒株疫苗,保护效果往往不理想,导致免疫失败。
1.5
混合感染与环境压力

与其他免疫抑制病共感染:IBDV经常与鸡传染性贫血病毒、马立克氏病病毒、呼肠孤病毒等其他免疫抑制病原发生混合感染,产生协同致病效应,导致比单一感染严重得多的后果。
环境中的病毒载量高:由于病毒抵抗力极强,经常在环境中长时间存活,在多年连续饲养的鸡场中,病毒载量不断累积,导致雏鸡早期感染的风险持续增高。
当前传染性法氏囊病毒的流行呈现多种基因型并存。因此,养殖场进行疫苗接种时,需要根据本地区的流行病学调查结果,选择包含流行毒株的疫苗,才能提供有效保护。
二、现有解决策略

疫苗接种是防控IBD的核心,但关键在于“精准”,而非盲目接种。
2.1
疫苗类型的选择

2.1.1活疫苗:
温和型:对法氏囊无损伤,但保护力有限,主要用于低毒力地区或基础免疫。
中等毒力型:目前全球最广泛使用的类型,能有效抵抗强毒攻击,但对法氏囊有轻微可逆的损伤。
中等偏强/强毒力型:仅在vvIBDV高发地区使用,保护力强,但对法氏囊损伤风险高,需谨慎使用。
2.1.2灭活疫苗:
主要用于种鸡开产前,刺激产生高而均匀的抗体,通过蛋传递给雏鸡,提供坚实的母源抗体保护。
2.1.3免疫复合物疫苗:
免疫复合物疫苗:将活病毒与特异性抗体结合,可以突破母源抗体干扰,实现早期、均匀免疫。
病毒样颗粒疫苗:安全、高效,能提供更广谱的保护,是未来的发展方向。
2.2
免疫程序的关键:监测与时机

疫苗选择考虑:必须根据本场或本地区的流行毒株进行选择。
在vvIBDV流行区,应使用中等偏强毒力疫苗。
在变异株流行区,应使用与流行株抗原匹配的疫苗(如某些特定血清型的疫苗或多价疫苗)。
监测母源抗体:这是制定免疫程序的基石。通过定期采集雏鸡血清,用ELISA方法检测母源抗体水平。
目标:找到母源抗体衰退到不足以提供保护的“窗口期”,并在此窗口期进行首次免疫。
好处:避免免疫过早(母源抗体中和疫苗病毒,导致免疫失败)或过晚(已发生野毒感染)。
三、威尼斯886699提供解决方案

3.1
利用Bac-to-Bac系统构建筛选表达
IBDV保护抗原的杆状病毒

用时:1-2个月
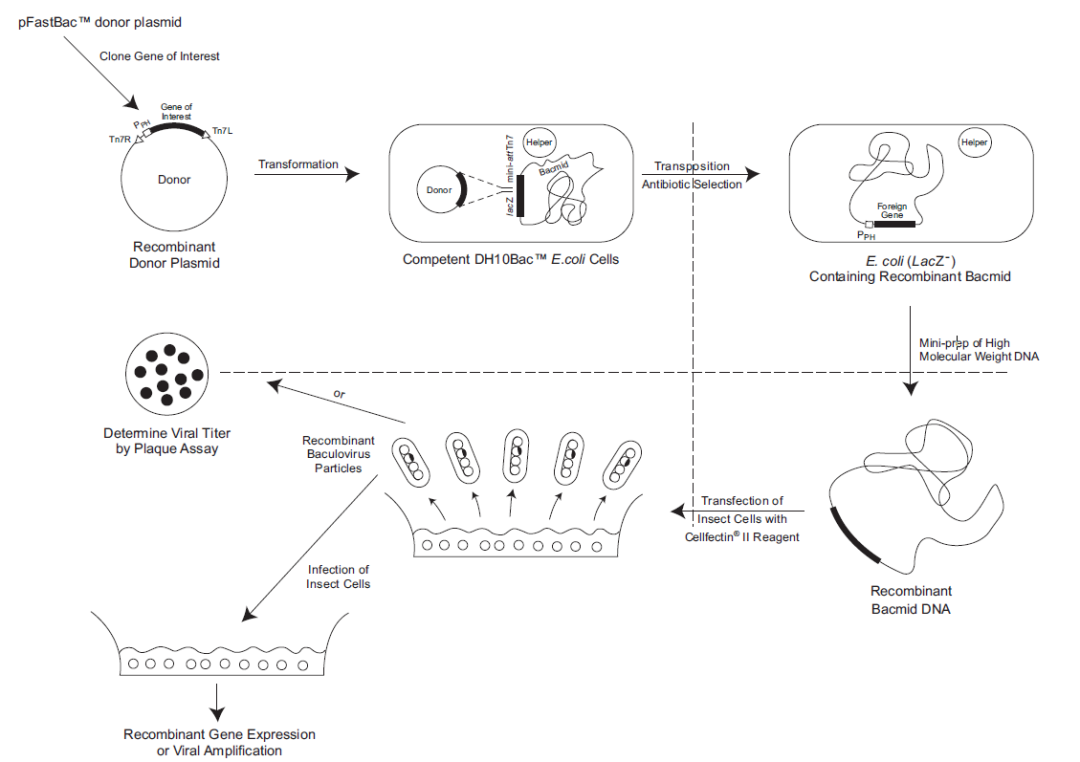
3.2
高表达昆虫-杆状病毒生产技术

昆虫细胞培养基
• 无血清全悬浮培养基
• 稳定维持昆虫细胞生长
• 广泛应用于SF9、High Five细胞的杆状病毒系统蛋白表达
• 支持细胞高密度生长、蛋白高效表达和大规模生产放大
用时:1个月
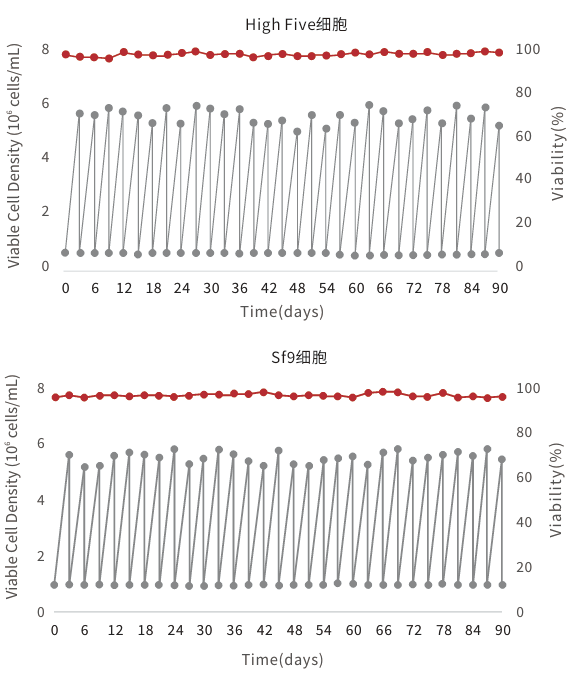
长期稳定传代,高密度生长,且活率维持在95%以上
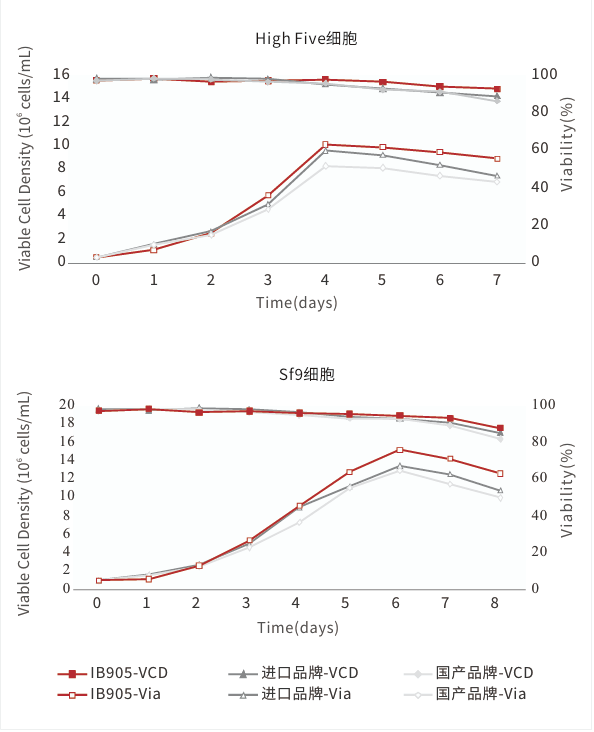
生长速率更快,密度更高,维持时间更长
3.3
工艺开发与放大

表达验证:使用SDS-PAGE、ELISA等技术验证VP2蛋白的正确表达和产量。
培养条件优化:在摇瓶和生物反应器中优化细胞培养条件(pH、温度、溶氧、feed策略),以提高蛋白表达量和细胞密度。
大规模悬浮培养:在50L-200L生物反应器中进行批次、流加或灌流培养,建立稳定可控的上游生产工艺。
后续纯化:将高浓度的纯化后的VP2蛋白与适宜的佐剂进行配苗,以增强免疫效果。
用时:约1-2月。
3.4
动物试验评价

安全性: 证明疫苗对靶动物(鸡)本身是安全的,不引起显著不良反应。
有效性: 证明疫苗能够刺激机体产生足够的免疫保护,有效预防法氏囊病毒感染和相关疾病。
效力: 确定疫苗产生保护作用所需的最小抗原剂量(最小免疫剂量)。
用时:2-3个月
综上,约3月即可获得最新亚型传染性法氏囊病毒(IBDV) VP2蛋白;约6月即可获得高表达水平VP2蛋白的稳定昆虫亚单位工程细胞株。
在实际生产中,两者常常互补使用,形成高效的免疫程序。例如:
“免疫复合物疫苗首免 + 活疫苗加强免疫”:利用免疫复合物疫苗突破母源抗体进行首免,奠定免疫基础;之后再用一次中等毒力活疫苗进行加强,刺激产生全面、坚强的保护力。这种组合策略兼顾了安全性与有效性,是现代养禽业防控IBD的先进方案。
 (0575) 8070 9355
(0575) 8070 9355
 (0575) 8070 9355
(0575) 8070 9355
 marketing@yskbio.com
marketing@yskbio.com
 浙江省绍兴市诸暨市陶朱街道聚力路16号
浙江省绍兴市诸暨市陶朱街道聚力路16号
©2023 版权所有
