mRNA 疫苗平台:从 COVID-19 应急突破到全球医疗健康新范式

圣诞快乐

Merry Christmas | Merry Christmas | Merry Christmas
在人类与传染病的漫长博弈中,疫苗始终是最锋利的 “防御武器”。从 18 世纪詹纳发明牛痘疫苗对抗天花,到 20 世纪脊髓灰质炎疫苗、乙肝疫苗的广泛应用,疫苗学的每一次突破都深刻改变着公共卫生格局。而 mRNA 疫苗在 COVID-19 疫情中的 “快速实现研发转化”,不仅创下了 “1 年内完成研发并获批上市” 的行业里程碑意义的突破,更以其独特的技术优势,打破了传统疫苗的研发边界,为传染病防控、癌症治疗乃至罕见病干预带来颠覆性可能。本文将深入解析 mRNA 疫苗平台的最新进展,探讨其超越 COVID-19 的应用前景与未来方向。同时,全球产业格局的重塑与政策层面的推动也将深刻影响 mRNA 技术的落地与普及。


mRNA 疫苗:疫情催生的 “技术破局者”

1. 疫苗学发展的 “三次革命”
回顾疫苗学的发展历程,可清晰看到三次关键技术跃迁:
第一次革命(减毒 / 灭活疫苗时代):以牛痘疫苗、脊髓灰质炎灭活疫苗为代表,通过弱化或杀死病原体激发免疫反应,优点是安全性较高,但研发周期长(通常 5-10 年),且对部分病毒(如 HIV)难以奏效。
第二次革命(基因工程疫苗时代):重组蛋白疫苗(如乙肝疫苗)、病毒载体疫苗(如埃博拉疫苗)通过基因工程技术表达病原体抗原,摆脱了对完整病原体的依赖,但仍受限于 “体外表达抗原” 的工艺复杂性。
第三次革命(核酸疫苗时代):mRNA 疫苗直接向人体细胞 “递送遗传指令”,让细胞自主合成抗原,实现了 “体内自主生产免疫原” 的突破。这种 “以细胞为工厂” 的模式,从根本上缩短了研发周期,也为多场景应用埋下伏笔。
此外,该阶段的成功为疫苗学研究提供了新的方法学范例,也推动了监管机构在加速审批路径上的探索。
2. COVID-19 中的 “里程碑时刻”
2020 年,COVID-19 疫情全球大流行,传统疫苗研发的 “慢节奏” 难以应对紧急公共卫生需求。此时,mRNA 疫苗凭借 “设计灵活、生产快速” 的优势脱颖而出:
辉瑞 / BioNTech(BNT162b2):2020 年 12 月获 FDA 紧急使用授权(EUA),III 期临床试验数据显示,对预防 COVID-19 感染的有效性达 95%,且在不同年龄、种族人群中表现稳定。截至 2023 年底,全球接种量超 35 亿剂,成为对抗 Delta、Omicron 等变异株的核心武器。
Moderna(mRNA-1273):同期获批的另一款 mRNA 疫苗,有效性达 94.1%,其研发团队仅用 2 天就完成了疫苗序列设计,从启动研发到进入临床试验仅耗时 2 个月,刷新了疫苗研发的 “速度纪录”。
这两款疫苗的成功,不仅验证了 mRNA 技术在传染病防控中的可行性,更让全球看到了该平台 “快速响应突发公共卫生事件” 的核心价值。

mRNA 疫苗的 “核心密码”:
结构优化与递送突破

mRNA 疫苗的成功,离不开两大技术支柱:精准的 mRNA 分子设计与高效的递送系统。二者共同解决了 mRNA 分子 “不稳定、易被降解、难入细胞” 的天然缺陷。
1. mRNA 分子的 “三重优化”
天然 mRNA 在人体内易被核酸酶降解,且会激活免疫系统的 “天然防御机制”(如 TLR3/TLR7 受体识别),引发非特异性炎症反应。为解决这些问题,科学家通过三项关键改造实现了 mRNA 的 “功能升级”:
修饰核苷技术:用假尿苷(Ψ)、N6 - 甲基腺苷(m6A)等修饰核苷替代天然尿苷,可显著降低 mRNA 的免疫原性(减少 80% 以上的炎症因子释放),同时提升其翻译效率(使抗原蛋白表达量增加 3-5 倍)。这一技术由 Pardi N. 团队在 2015 年突破,成为 mRNA 疫苗研发的 “基石”(Pardi N. et al., 2020, Vaccines 8 (1):17)。
5′帽子结构(m7GpppNm):模拟真核生物 mRNA 的天然帽子结构,不仅能避免 mRNA 被 5′- 核酸酶降解,还能招募核糖体启动翻译过程,使 mRNA 的半衰期延长至 48 小时以上(天然 mRNA 半衰期通常不足 1 小时)。
3′poly (A) 尾巴:通过优化 poly (A) 尾巴的长度(通常 50-100 个腺苷酸),进一步增强 mRNA 的稳定性,同时促进核糖体结合,提升抗原蛋白的表达效率。
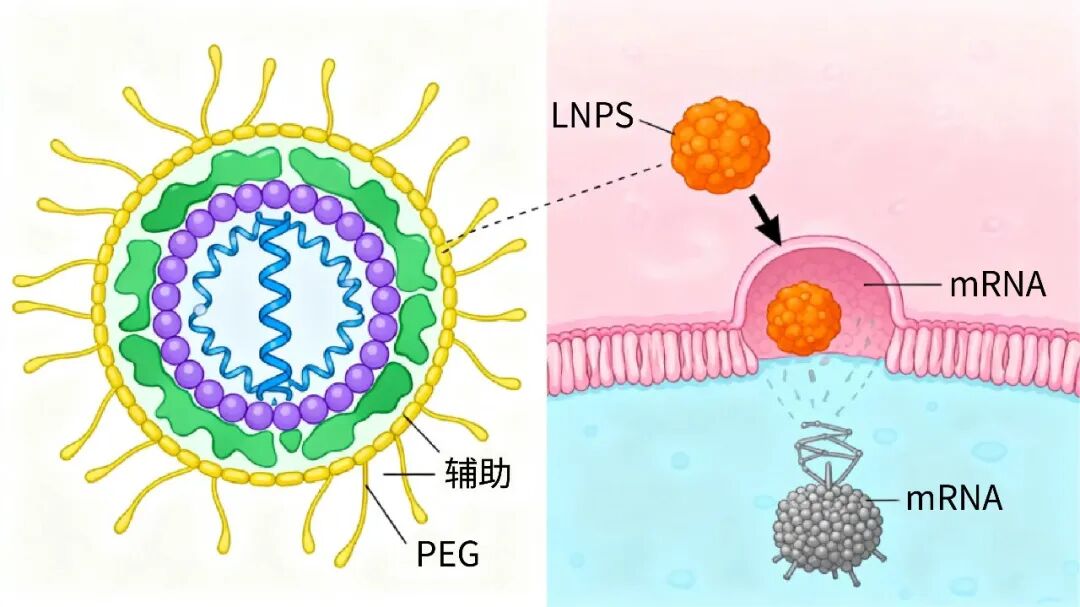
2. 脂质纳米颗粒(LNPs):mRNA 的 “保护神”
mRNA 分子带负电且水溶性强,难以穿透同样带负电的细胞膜。脂质纳米颗粒(LNPs)的出现,完美解决了这一 “递送难题”。目前获批的 mRNA 疫苗均采用 LNPs 递送系统,其核心优势体现在:
“四层结构” 的保护机制:LNPs 由可离子化脂质、磷脂、胆固醇和 PEG 化脂质组成,形成直径约 100nm 的球形颗粒。其中,可离子化脂质在酸性环境(如内体)中带正电,与带负电的 mRNA 结合形成复合物;胆固醇维持颗粒稳定性;PEG 化脂质减少免疫系统清除,延长体内循环时间。
“精准靶向” 细胞:LNPs 通过内吞作用进入树突状细胞、巨噬细胞等免疫细胞,在细胞内释放 mRNA,使其顺利启动抗原合成。研究显示,LNPs 递送的 mRNA 在免疫细胞中的转染效率比裸 mRNA 提升 1000 倍以上(Creech C.B. et al., 2022, Vaccines 10 (2):208)。
可调控的生物分布:通过调整脂质成分比例,可改变 LNPs 的靶向器官(如肝脏、肺部),为 mRNA 疫苗在非传染病领域的应用(如肝脏罕见病)提供可能。

从 “应急防控” 到 “多病种覆盖”:
mRNA 疫苗的应用扩张

COVID-19 的成功只是 mRNA 技术的 “首秀”,目前全球已有数十款 mRNA 疫苗进入临床试验,覆盖传染病、癌症、自身免疫病等多个领域,展现出 “一平台多用途” 的强大潜力。
1. 传染病防控:覆盖 “传统疫苗难以攻克” 的病毒
mRNA 疫苗的 “快速设计” 优势,使其成为对抗变异频发、新发突发传染病的 “理想选择”,除 COVID-19 外,多个领域已取得突破性进展:
狂犬病疫苗:Moderna 的 mRNA 狂犬病疫苗(mRNA-1215)在 I 期临床试验中,仅需一剂接种就诱导出比传统灭活疫苗更强的中和抗体反应(滴度达 WHO 保护标准的 10 倍以上),且安全性良好。目前已进入 II 期临床,有望替代需多次接种的传统疫苗。
流感疫苗:传统流感疫苗需每年根据流行毒株 “猜测性” 研发,有效性波动较大(20%-60%)。mRNA 流感疫苗(如辉瑞的 PF-07252220)可同时表达 4 种流感病毒抗原(H1N1、H3N2、甲型 H5N1、乙型 Victoria),实现 “四价覆盖”。I/II 期数据显示,其诱导的中和抗体滴度比传统疫苗高 2-3 倍,且研发周期可缩短至 8 周,大幅提升流感防控效率。
寨卡疫苗:BioNTech 的寨卡 mRNA 疫苗(BNT1641)在动物实验中,可诱导强烈的中和抗体反应,完全保护小鼠免受寨卡病毒攻击,目前已进入 I 期临床,为热带地区传染病防控提供新方案。
2. 癌症治疗:“个体化” 的精准免疫武器
癌症疫苗的核心思路是 “激活人体自身免疫系统识别并清除癌细胞”,而 mRNA 技术的出现,让 “个体化癌症疫苗” 从概念走向现实:
个体化新抗原疫苗:癌细胞会产生独特的 “新抗原”(由基因突变产生),mRNA 疫苗可根据患者肿瘤的基因测序结果,快速设计并合成针对这些新抗原的 mRNA 序列。例如,BioNTech 的个性化癌症疫苗(BNT122)在黑色素瘤患者中开展的 II 期临床显示,联合 PD-1 抑制剂(Keytruda)治疗后,患者的无进展生存期(PFS)比单独使用 PD-1 抑制剂延长 50%,且 60% 的患者实现肿瘤缩小。
共享抗原疫苗:针对肺癌、乳腺癌等常见癌症中 “共享” 的肿瘤抗原(如 NY-ESO-1、MAGE-A3),mRNA 疫苗可实现 “通用化” 生产。Moderna 的 mRNA-4157(针对 20 种共享抗原)在晚期黑色素瘤患者中,联合 Keytruda 的客观缓解率(ORR)达 50%,显著高于单独使用 Keytruda 的 36%。
3. 非传染性疾病:突破 “传统疗法局限”
mRNA 疫苗不仅能 “激活免疫”,还可通过调控免疫反应或补充功能蛋白,用于治疗自身免疫病、过敏、罕见病等非传染性疾病:
自身免疫病:针对类风湿关节炎、多发性硬化症等疾病,mRNA 疫苗可设计为 “抑制过度免疫反应” 的 “ tolerogenic 疫苗”。例如,利用 mRNA 表达自身抗原片段,诱导调节性 T 细胞(Treg)分化,从而抑制炎症反应。目前,德国 BioNTech 与美国 Vertex 合作的 mRNA 自身免疫病疫苗已进入临床前研究。
罕见病:对于因基因缺陷导致的蛋白缺乏型罕见病(如囊性纤维化、血友病),mRNA 疫苗可作为 “蛋白替代疗法” 的载体,向患者体内递送编码功能蛋白的 mRNA。例如,Moderna 的 mRNA 血友病 B 疫苗(mRNA-6231)在动物实验中,可使凝血因子 IX 水平提升至正常水平的 30% 以上,有望替代需终身注射的凝血因子制剂。

前行中的 “主要技术与产业瓶颈”:
mRNA 疫苗面临的挑战

尽管 mRNA 疫苗展现出广阔前景,但其商业化和普及仍面临三大核心瓶颈,亟待技术突破和产业升级。
1. 稳定性与储存:“冷链依赖” 制约普及
mRNA 分子本质是单链核酸,对温度极为敏感,目前已上市的 mRNA 疫苗均需严格冷链储存:
辉瑞 / BioNTech 疫苗需在 -80℃ 至 -60℃ 条件下储存,解冻后在 2-8℃环境中仅能保存 5 天;
Moderna 疫苗虽可在 -20℃储存 6 个月,但在室温下仅能稳定 4 小时。这种 “冷链依赖” 不仅增加了运输和储存成本(全球冷链物流成本占疫苗总成本的 30%-50%),更限制了其在冷链基础设施薄弱的发展中国家的应用。据 WHO 统计,截至 2023 年,低收入国家 mRNA 疫苗接种率不足 15%,远低于高收入国家的 60% 以上。
2. 长期安全性与免疫耐受
mRNA 疫苗的短期安全性已通过大规模接种验证(常见不良反应为注射部位疼痛、发热,发生率约 10%-20%),但长期安全性(如对生殖系统、免疫系统的潜在影响)仍需更长时间的监测:
目前最长的随访数据显示,接种 mRNA 疫苗 2 年后,未发现明确的长期不良反应,但针对特殊人群(如孕妇、免疫缺陷者)的安全性数据仍不充分;部分患者在接种后出现 “免疫疲劳” 现象,即多次加强针后抗体水平提升不明显,提示可能存在免疫耐受问题,需通过疫苗佐剂优化或递送系统改进解决。
3. 生产与公平分配:“产能壁垒” 加剧全球失衡
mRNA 疫苗的生产工艺复杂,对技术和设备要求极高,导致产能集中在少数发达国家。
生产核心环节(如 mRNA 合成、LNPs 制备)需依赖专用设备(如连续流反应器)和高纯度原料(如修饰核苷、可离子化脂质),目前全球仅 10 余家企业具备规模化生产能力。
截至 2023 年,全球 mRNA 疫苗年产能约 100 亿剂,但 80% 以上集中在欧美企业,发展中国家难以获得技术转让和产能支持,导致 “疫苗民族主义” 加剧,全球公共卫生安全面临挑战。同时,全球产业格局的重塑与政策层面的推动也将深刻影响 mRNA 技术的落地与普及。

未来方向:
技术创新引领 mRNA 疫苗 “升级换代”

为突破现有瓶颈,全球科研机构和企业正从分子设计、递送系统、研发模式等多维度发力,推动 mRNA 疫苗进入 “2.0 时代”。
1. 新一代 mRNA 分子:更稳定、更高效
自放大 RNA(saRNA):在传统 mRNA 基础上插入 “复制酶基因”,使其进入细胞后可自主复制,实现 “一剂接种即持续表达抗原”。研究显示,saRNA 疫苗的抗原表达量比传统 mRNA 高 10-100 倍,可减少接种剂量(从 100μg 降至 10μg),同时降低生产成本。目前,美国 Vaxart 公司的 saRNA 流感疫苗已进入 I 期临床。
环状 RNA(circRNA):通过分子内连接形成环状结构,彻底解决了 mRNA 被核酸酶降解的问题,其半衰期可达传统 mRNA 的 10 倍以上,且无需冷链储存(室温下可稳定 7 天)。中国苏州瑞博生物的 circRNA 新冠疫苗已进入临床前研究,有望成为首个 “常温储存” 的 mRNA 疫苗。
2. 多价疫苗与联合策略:“一苗防多病”
多价传染病疫苗:将多种病原体的抗原 mRNA 整合到同一 LNPs 中,实现 “一剂接种预防多种疾病”。例如,Moderna 正在研发的 “新冠 + 流感 + RSV 三联疫苗”,已在动物实验中诱导出针对三种病毒的高滴度中和抗体,预计 2025 年进入临床试验。
联合疗法增效:除与免疫检查点抑制剂联合治疗癌症外,mRNA 疫苗还可与 CAR-T 细胞疗法、溶瘤病毒等联合,形成 “协同杀伤癌细胞” 的网络。例如,BioNTech 的 mRNA 疫苗联合 CAR-T 细胞治疗淋巴瘤,在临床前研究中使肿瘤完全消退率提升至 80%(单独 CAR-T 治疗为 40%)。
3. 人工智能(AI):加速疫苗研发 “全流程”
AI 技术正深度融入 mRNA 疫苗的设计、优化和筛选环节,大幅缩短研发周期:
抗原预测:通过 AI 模型(如 AlphaFold2)分析病原体蛋白结构,精准预测 “最易被免疫系统识别” 的抗原片段,减少筛选工作量。例如,DeepMind 利用 AI 预测的新冠病毒刺突蛋白抗原,与实际有效抗原的匹配度达 95% 以上。
mRNA 序列优化:AI 可根据密码子偏好性、mRNA 二级结构等参数,自动设计最优序列,使抗原表达效率提升 2-3 倍。Moderna 利用自主研发的 AI 平台(mRNA Design Studio),将疫苗序列设计时间从 2 周缩短至 1 天。
临床试验设计:AI 通过分析历史临床数据,可优化受试者招募方案、预测临床试验结果,使 III 期临床试验周期缩短 30%-40%。

结论与展望

mRNA 疫苗在 COVID-19 疫情中的成功,不仅是一次 “应急技术突破”,更是医疗健康领域的 “范式革命”。从传染病防控到癌症治疗,从罕见病干预到自身免疫病调节,mRNA 技术正以 “平台化、多用途” 的特性,重构人类对抗疾病的 “武器库”。
尽管稳定性、产能、公平分配等挑战仍需解决,但随着 saRNA、circRNA、AI 设计等技术的突破,mRNA 疫苗有望在未来 5-10 年实现 “三大跨越”:从 “冷链依赖” 走向 “常温储存”,从 “单病种覆盖” 走向 “多价通用”,从 “发达国家主导” 走向 “全球公平可及”。
对于生物制药行业而言,mRNA 技术的崛起也带来了新的机遇:一方面,其 “快速研发、灵活生产” 的特性,将推动疫苗企业从 “传统生产型” 向 “技术服务型” 转型;另一方面,mRNA 与基因编辑、细胞治疗等技术的融合,可能催生 “下一代精准医疗方案”。正如 Sahin U. 团队在研究中指出的:“mRNA 技术的潜力远未被充分挖掘,它将成为未来 20 年医疗健康领域最具变革性的平台之一”
在这场技术革命中,中国企业正加速追赶:从自主研发的 mRNA 新冠疫苗获批紧急使用,到 circRNA、saRNA 技术进入临床前研究,再到 LNPs 递送系统的国产化突破,中国正逐步在 mRNA 领域形成 “从基础研究到产业落地” 的完整链条。未来,随着产学研协同创新的深化,mRNA 疫苗有望不仅成为 “公共卫生的核心支撑”,更成为推动中国生物制药产业 “弯道超车” 的核心力量。

参考文献

[1].Pardi N, Hogan MJ, Porter FW, Weissman D. mRNA vaccines — a new era in vaccinology[J]. Nature Reviews Drug Discovery, 2018, 17(4):261-279.
[2].Polack F P, Thomas S J, Kitchin N, et al. Safety and Efficacy of the BNT162b2 mRNA COVID-19 Vaccine[J]. The New England Journal of Medicine, 2020, 383(27):2603-2615.
[3].Baden L R, El Sahly H M, Essink B, et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine[J]. The New England Journal of Medicine, 2021, 384(5):403-416.
[4].Hou X, Zaks T, Langer R, Dong Y. Lipid nanoparticles for mRNA delivery[J]. Nature Reviews Materials, 2021, 6(11):1078-1094.
[5].Sahin U, Karikó K, Türeci Ö. mRNA-based therapeutics — developing a new class of drugs[J]. Nature Reviews Drug Discovery, 2014, 13(10):759-780.
 (0575) 8070 9355
(0575) 8070 9355
 (0575) 8070 9355
(0575) 8070 9355
 marketing@yskbio.com
marketing@yskbio.com
 浙江省绍兴市诸暨市陶朱街道聚力路16号
浙江省绍兴市诸暨市陶朱街道聚力路16号
©2023 版权所有
