人多能干细胞(hPSC)培养常见问题及解决思路

科学与技术
hPSC培养
01
细胞贴壁不良/死亡率高
可能原因:
基质(Matrigel、Laminin、Vitronectin 等)浓度不足或失活
传代方法过于粗暴,细胞损伤严重
ROCK 抑制剂未使用或撤掉过早
解决思路:
确保基质正确稀释与铺板,避免冻融过多次
建议使用 EDTA 温和消化,避免完全单细胞化,酶消化对于细胞损伤较大,长期也容易导致分化
一般复苏时要加入ROCK抑制剂,帮助细胞第一天贴壁,后续换液就可以不再加入,如果后续仍出现贴壁不良的情况,也可以尝试继续在培养基中加入ROCK抑制剂
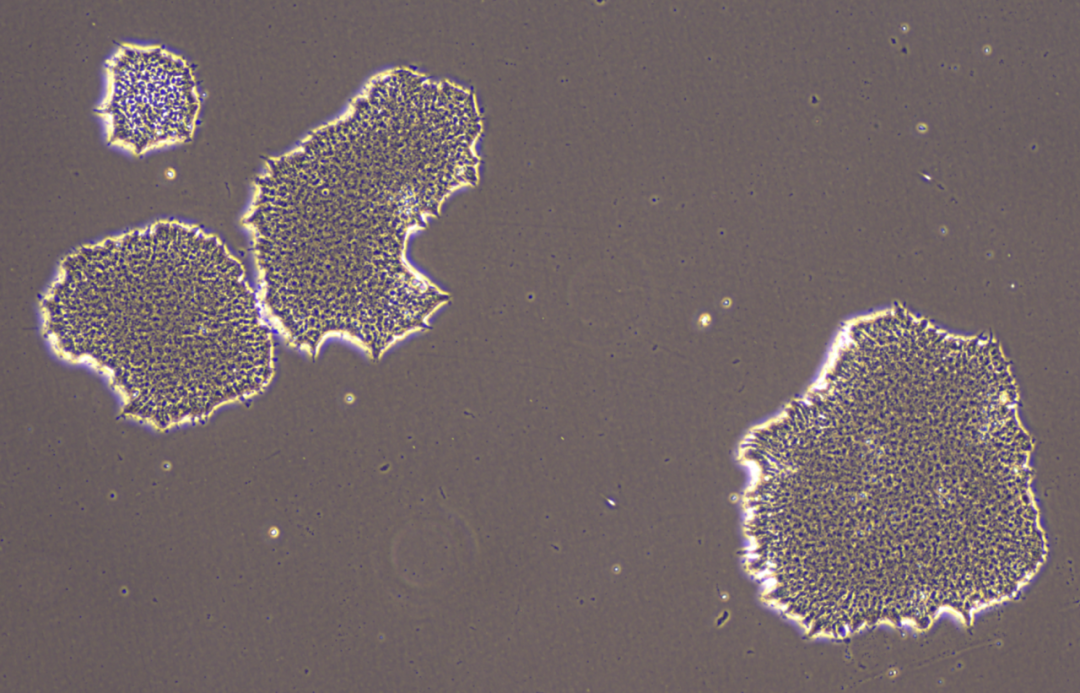
健康的hPSC核/质比高,核仁明显,多个核仁,能形成紧凑的克隆团,细胞扁平且密集,克隆团边缘清晰光滑。下图是Stem-Ex hPSC维持培养基培养的H9细胞。
02
细胞过度分化
可能原因:
培养基失效或成分不均一
培养密度过低或过高,细胞间信号失衡
传代间隔过长,细胞过度融合
解决思路:
确保培养基新鲜,不超过2周,冻存组分不能反复冻融
合理控制接种密度(一般 20–40% 汇合度最佳)
保持 3–5 天传代,避免过度长时间培养
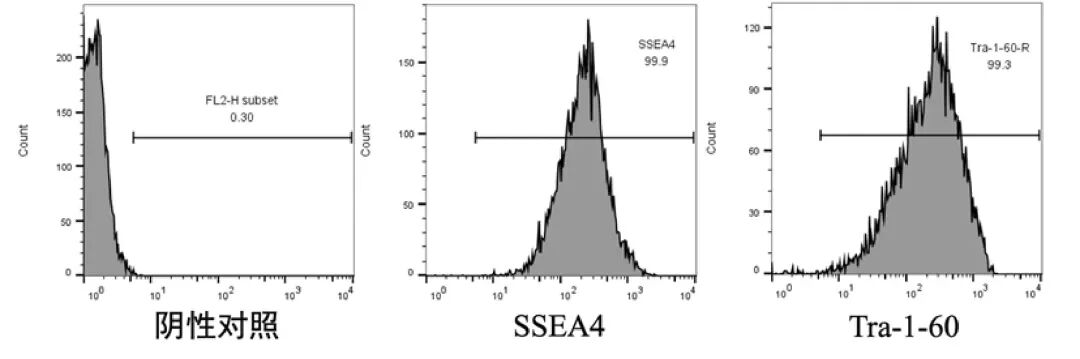
常见的多能性指标有SSEA4,Tra-1-60等,在Stem-Ex hPSC维持培养基中,多代培养后,hPSC的多能性指标超过99%。
03
细胞形态异常
表现:
细胞拉长、扁平,失去典型圆形/紧密集落
集落边缘细胞散开,分化趋势明显
可能原因:
基质浓度不均,铺板不完整
细胞张力过大,分化诱导
培养基受污染或成分不稳定
解决思路:
检查基质涂层是否均匀
确认培养基批次稳定性
排查污染:细菌、真菌、支原体
重新复苏细胞培养
04
支原体污染
常见表现:
细胞生长缓慢,形态异常
培养液 pH 异常或变浑浊
解决思路:
定期做支原体检测(qPCR、荧光染料)
污染严重时需丢弃细胞系,避免交叉感染
05
冻存/复苏后活率低的一些解决思路
冻存过程:
冻存对数生长期的细胞,一般在传代后2-4天,略早于传代时间
注意消化处理,冻存的细胞团直径在50-200微米
注意冻存程序,如使用冻存盒,不要在-80度放置太久
复苏过程:
使用和冻存前一致的培养体系,包括培养基和包被基质。如要更换体系,在复苏后第二代,可尝试梯度更换
复苏后第一代,培养基中要加入ROCK抑制剂
重悬时,细胞先加入离心管,向细胞沉淀中逐滴加入培养基
 (0575) 8070 9355
(0575) 8070 9355
 (0575) 8070 9355
(0575) 8070 9355
 marketing@yskbio.com
marketing@yskbio.com
 浙江省绍兴市诸暨市陶朱街道聚力路16号
浙江省绍兴市诸暨市陶朱街道聚力路16号
©2023 版权所有
